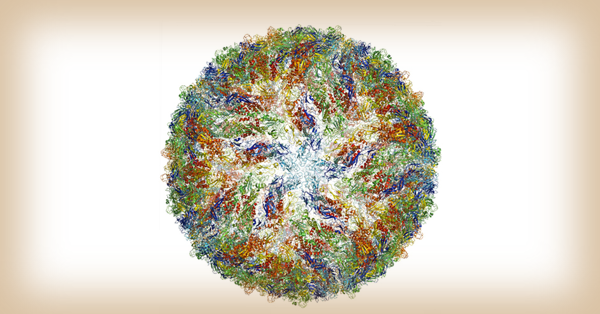
প্রথম পর্বে আলোচনা করেছিলাম কীভাবে ক্রায়ো-ইলেকট্রন মাইক্রোস্কোপ বা ক্রায়ো-ইএম জৈব অণুদের খুব তাড়াতাড়ি -১৫০ ডিগ্রী সেলসিয়াস তাপমাত্রার নিচে ঠান্ডা করে স্পষ্ট ত্রিমাত্রিক বা 3D ছবি তুলতে পারে। ইবোলা, জিকা ইত্যাদি ভাইরাসের ও ক্যান্সারের ছবি তুলে ক্রায়ো-ইএম চিকিৎসাশাস্ত্রে ও গবেষণার জগতে যুগান্তর এনেছে।
ক্রায়ো-ইলেকট্রন মাইক্রোস্কোপ আবিষ্কারের ইতিবৃত্ত
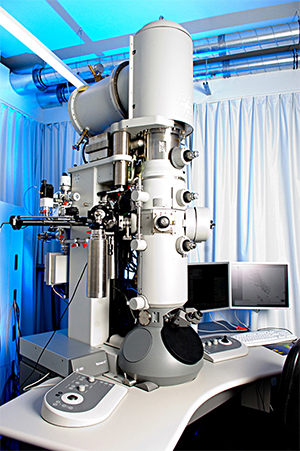
‘ক্রায়ো-ইএম’-এর এই ”এলেন, দেখলেন ও জয় করলেন” অবস্থা একদিনে তৈরী হয়নি। ১৯৬০-এর দশকের শেষের দিকে স্কটিশ মলিকুলার বায়োলজিস্ট রিচার্ড হেন্ডারসন কেমব্রিজ বিশ্ববিদ্যালয় থেকে এক্স-রে ক্রিস্টালোগ্রাফি দিয়ে প্রোটিনের কাঠামো বের করার উপর পিএইচডি করেন। এরপর তিনি কেমব্রিজের মেডিকেল রিসার্চ কাউন্সিল’স ল্যাবরেটরি অফ মলিকুলার বায়োলজিতে ইলেক্ট্রন মাইক্রোস্কোপের সাহায্যে ব্যাক্টেরিয়োরোডোপ্সিনের গঠন বোঝার চেষ্টা করেন।৫ কিন্তু, মুশকিল হলো প্রতিবারেই ব্যাক্টেরিয়োরোডোপ্সিন ইলেকট্রন মাইক্রোস্কোপ যন্ত্রে ব্যবহৃত উচ্চশক্তির ইলেক্ট্রনের স্রোত ও অতি-শূন্যতায় (vacuum) ভেঙে যাচ্ছিল। তাই হেন্ডারসন গ্লুকোজ দ্রবণের আস্তরণ বা কোটিং দিয়ে ব্যাক্টেরিয়োরোডোপ্সিন-কে সুরক্ষিত করে ইলেক্ট্রন মাইক্রোস্কোপের মধ্যে ব্যবহার করলেন। একইসঙ্গে তিনি ইলেক্ট্রন স্রোতের শক্তিও কমিয়ে দিলেন। কিন্তু এতসবের পরও হেন্ডারসন খুব একটা স্পষ্ট ছবি পেলেন না। তবে এই কোটিং পদ্ধতি তাঁর মনে ধরলো। তখন ১৯৭৫ সাল। পরের কয়েক বছরের মধ্যে হেন্ডারসন উদ্ভাবন করলেন ‘কুলিং টেকনোলজি’। ব্যাক্টেরিয়োরোডোপ্সিনকে তরল নাইট্রোজেনের মধ্যে জমিয়ে ১৯৯০ সালে সূচনা করলেন ক্রায়ো-ইএম- এর। ছবির স্পষ্টতাও বেড়ে গেল! কিন্তু তা তো শুধুমাত্র একটি প্রোটিনের মধ্যে সীমাবদ্ধ থাকলে চলবে না। শুরু হলো আরো গভীর গবেষণা।
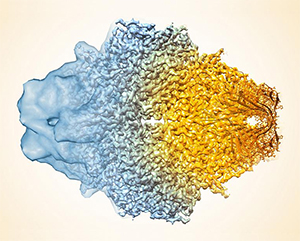
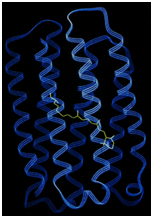
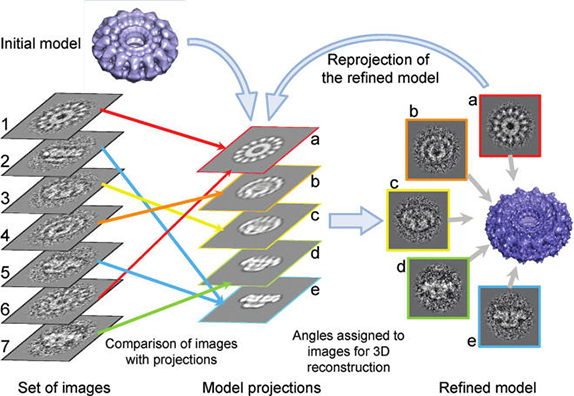
১৯৮২ সালে সুইস বিজ্ঞানী জ্যাক দুবোসে ইউনিভার্সিটি অফ লুসানে আবিষ্কার করলেন ‘ভিট্রিফিকেশন’ পদ্ধতি। খুব তাড়াতাড়ি জলকে তরল নাইট্রোজেনে (−১৯৫.৭৯ °C) ঠান্ডা করে কঠিনে পরিণত করাই হলো ‘ভিট্রিফিকেশন’। প্রোটিনের জলীয় দ্রবণ ‘ভিট্রিফিকেশন’ এর সাহায্যে কঠিন পরিণত হলো। আগেই বলেছি, এই ভিট্রিফায়েড নমুনা প্রোটিনের মধ্যে থাকা জমা জলের অণুই ক্রায়ো-ইএমে ব্যবহৃত প্রোটিনের সুরক্ষার বর্ম। এই সুরক্ষাই ছিল হেন্ডারসনের কাছে ‘মোস্ট ওয়ান্টেড’! আশির দশকের মাঝামাঝি জার্মান বিজ্ঞানী জোয়াকিম ফ্রাঙ্ক তৈরী করলেন এক উন্নততর অ্যালগোরিদম যা অনেক দ্বিমাত্রিক বা 2D ছবির প্রক্রিয়াকরণ (image processing) করে এক স্পষ্ট ত্রিমাত্রিক বা 3D ছবি বের করে আনে। প্রথমে প্রাপ্ত অসংখ্য দ্বিমাত্রিক ছবিগুলিকে সিগন্যাল-টু-নয়েস রেসিও (Signal to Noise ratio) বাড়িয়ে শ্রেণীকরণ (classify) করা হয়। ছবিগুলির প্রজেকশন অনুযায়ী তুলনা করে (চিত্র ৪) একই রকম ছবিগুলিকে শ্রেণীবদ্ধ করার জন্য আধুনিক অ্যালগোরিদমের সাহায্য নেওয়া হয়। এরপর শ্রেণীবদ্ধ 2D ছবিগুলিকে বিভিন্ন কোণে বিন্যস্ত করে উচ্চ স্পষ্টতা সম্পন্ন ত্রিমাত্রিক বা 3D মডেল পাওয়া যায়।৯
চিকিৎসাশাস্ত্রে ইউরেকা
জিকা ভাইরাস ও ক্রায়ো-ইএম
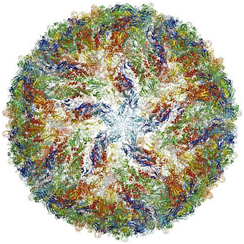
চিত্র ৫ – ক্রায়ো-ইলেক্ট্রন মাইক্রোস্কোপে দৃশ্যমান জিকা ভাইরাস। ছবির উৎস Johan Jarnestad/The Royal Swedish Academy of Sciences
টাইম মেশিনে চড়ে পিছিয়ে যাওয়া যাক ২০১৪ সালের অগাস্ট মাসে। ব্রাজিল আন্তর্জাতিক ক্যানুইং প্রতিযোগিতায় যোগ দিতে আসা কোনো অতিথির মাধ্যমে ছড়িয়ে পড়ে এক অজানা ভাইরাস। মৃত্যুর কোলে ঢলে পড়ল গর্ভস্থ ভ্রূণ ও সদ্যজাতকেরা। ব্রাজিল এবং পুরো ল্যাটিন আমেরিকাতে মহামারীর আকার নেয় এই ভাইরাসের আক্রমণ। সেই পরিস্থিতিতে একান্ত প্রয়োজন ছিল ভাইরাসটিকে চেনা ও তার প্রতিষেধক আবিষ্কার করা। এক্স-রে-ক্রিস্টালোগ্রাফি বা NMR পদ্ধতি দিয়ে চেষ্টা করা হল, কিন্তু এই ভাইরাসটাকে চেনা সম্ভবই হচ্ছিল না। এখানেই ক্রায়ো-ইএমের কারসাজি শুরু। নির্ভুলভাবে চেনা গেল এই ‘জিকা ভাইরাস’ আর তার মাস তিনেকের মধ্যেই আবিষ্কৃত হলো জিকা ভাইরাসের প্রতিষেধক।১০ ২০১৬-তে থামানো গেলো সদ্যোজাতের মৃত্যুযজ্ঞ।
ক্রায়ো-ইএমের সাহায্যে একে একে ইবোলা, ডেঙ্গু, এইডস বা সিভিয়ার ইনফ্লুয়েঞ্জার মতো জটিল রোগের ভাইরাসগুলির ছবি তোলা গিয়েছে। এর ফলে তাদের প্রতিষেধক ঔষধ আবিষ্কারের পথও সুগম হয়েছে। এজন্যই আমেরিকান কেমিক্যাল সোসাইটির সভাপতি অ্যালিসন ক্যাম্পবেলের মতে ক্রায়ো-ইএম যেন প্রকৃত অর্থে শরীরে ভাইরাসের গতিবিধি বোঝার ‘গুগল আর্থ’।১১
“ক্রায়ো-ইএম যেন প্রকৃত অর্থে শরীরে ভাইরাসের গতিবিধি বোঝার ‘গুগল আর্থ’।” – অ্যালিসন ক্যাম্পবেল, আমেরিকান কেমিক্যাল সোসাইটির সভাপতি
ক্যান্সার ও ক্রায়ো-ইএম
মানবদেহে ডিএনএ পুনরাবৃত্তি (DNA রেপ্লিকেশন) একটি সুশৃঙ্খল পদ্ধতি যা একটি কোষ থেকে আরেকটি কোষে জেনেটিক কোড অণুলিপি করে। এর ফলে জিনগত নির্দেশাবলী এক প্রজন্মের কোষ থেকে পরবর্তী প্রজন্মের কোষে পৌঁছয়। শরীরে যখন এই স্বাভাবিক জিনগত পরিবর্তন ও ডিএনএ রেপ্লিকেশন বাধা পায় তখন তৈরী হয় ক্যান্সার। ক্যান্সারের ফলে শরীরে অস্বাভাবিক কোষ লাগামছাড়াভাবে বাড়তে থাকে ও ত্রুটিপূর্ণ জেনেটিক রেপ্লিকেশন হতে থাকে। ক্রায়ো-ইএম ক্যান্সার কোষে এই ডিএনএ রেপ্লিকেশন সম্পর্কে অনেক তথ্য দিয়ে ক্যান্সার গবেষণাকে সমৃদ্ধ করেছে। ক্যান্সারের রোগীর শরীরে জিনের মিউটেশনে বড় ভূমিকা নেয় দুটি প্রোটিন — আইসোসাইট্রেট ডিহাইড্রোজিনেজ-১ (IDH-1) ও ল্যাকটেট ডিহাইড্রোজিনেজ (LDH)। IDH-1 ও LDH স্বাভাবিক অবস্থাতে কোনো সমস্যা সৃষ্টি না করলেও এদের মিউটেটেড অবস্থাতে সমস্যা শুরু হয়। IDH-1-এর মিউটেশনের ফলে উৎসেচকের স্বাভাবিক কার্যকলাপ ব্যাহত হয় ও প্রচুর ২-হাইড্রক্সিগ্লুটারেট (2-HG) তৈরী হয়। এর ফলে ডিএনএ মিথাইলেশন ব্যাহত হয় ও টিউমারজেনেসিস তথা ক্যান্সার এর সূত্রপাত হয়।১২ এছাড়াও, IDH-1 জিনের মিউটেশনের মাধ্যমে এই দুটি প্রোটিন ক্যান্সার রোগীর জিনের সজ্জায় অদলবদল ঘটায়, আর তার ফলে ব্যবহৃত ঔষধগুলি শরীরে অকেজো হয়ে যায়। ক্রায়ো-ইএম এই IDH-1, LDH ও তাদের মিউটেটেড অবস্থার প্রমান, গঠন ও আচার-আচরণ সম্পর্কে তথ্য দিয়ে ক্যান্সার গবেষণাকে সহজতর করে তুলেছে।
ক্রায়ো-ইএম ক্যান্সার গবেষণাকে সহজতর করে তুলেছে।
শুধু ক্যান্সার বা ভাইরাস নয়, ক্রায়ো-ইএম মানবদেহে আলঝাইমার্সের জন্য দায়ী অ্যামাইলয়েড পেপটাইডের গঠন কাঠামো ও শরীরে তাদের সমাবেশ সম্পর্কে অনেক তথ্য দিয়ে আলঝাইমার্সের গবেষণায় অনেক রহস্য উদ্ঘাটিত করেছে। এইসব কারণের জন্যই নোবেল কমিটি একে যুগান্তকারী আবিষ্কারের আখ্যা দিয়েছে।
(সমাপ্ত)
(প্রচ্ছদের ছবি: ক্রায়ো-ইলেক্ট্রন মাইক্রোস্কোপে দৃশ্যমান জিকা ভাইরাস, সূত্র: Johan Jarnestad, The Royal Swedish Academy of Sciences)
রেফারেন্স ও আরো বিশদে জানতে :
(১) Nature 2017, 550, 167.
(২) The Rise of Cryo-Electron Microscopy, spring 2016, 13-21.
(৩) https://en.wikipedia.org/wiki/Cryogenics
(৪) এক্ষেত্রে ক্রিস্টাল ও কাচ বা গ্লাসের গঠনগত পার্থক্য আলোচনা করলে ভিট্রিফিকেশন পদ্ধতির ধারণাটা পরিষ্কার হবে। কোনো দ্রবণকে দ্রুত জমিয়ে (quenched) ভিট্রিফিকেশন পদ্ধতিতে কাচ তৈরি হয়। এই দ্রুত জমিয়ে কঠিনে পরিণত হওয়ার ফলে দ্রবণের অণুগুলি স্থিতিশীল সজ্জায় (equilibrium configuration) আসার সময় পায় না — বিশৃঙ্খল (disordered) অবস্থাতেই কঠিনে পরিণত হয়। অন্যদিকে, ক্রিস্টাল কোনো দ্রবণ থেকে ধীরে ধীরে ঠান্ডা হওয়ার মাধ্যমে গঠিত হয় সংশ্লিষ্ট অণুগুলি একটি স্থিতিশীল সজ্জা পাওয়ার জন্য পর্যাপ্ত সময় পায়। সুতরাং, এক্ষেত্রে একটি সুশৃঙ্খল অণুসমষ্টির কেলাস বা ক্রিস্টাল তৈরী করে।
যদিও তরল নাইট্রোজেনের তাপমাত্রা অনেক কম (-১৯৫.৭৯ °C), ভিট্রিফিকেশন পদ্ধতিতে বর্তমানে তরল নাইট্রোজেন ব্যবহৃত হয় না। তরল নাইট্রোজেনের তাপ ধারণ ক্ষমতা ও তাপ পরিবাহিতা অনেক কম হওয়ায়, যখন কোনো সাধারণ তাপমাত্রার জলীয় দ্রবণ এর মধ্যে ফেলে দেওয়া হয়, তা গরম হয়ে ফুটতে শুরু করে এবং তা ভিট্রিফিকেশন পদ্ধতিকে মন্দীভূত করে। তরল নাইট্রোজেনের মাধ্যমে ভিট্রিফিকেশনের জন্য সময় বেশি লাগাতে এই পদ্ধতিতে ‘ভিট্রিফায়েড’ জলের পাশাপাশি বরফের ঘনক তৈরির সুযোগ থাকে। এক্ষেত্রে তরল ইথেনের তাপ ধারণ ক্ষমতা ও তাপ পরিবাহিতা তরল নাইট্রোজেনের তুলনায় বেশি, যদিও তাপমাত্রা মোটামুটি একই (-১৮৮ °C)। তাই, দ্রুত ও সঠিক ভাবে জৈব অণুর জলীয় দ্রবণকে ভিট্রিফিকেশনের জন্য বর্তমানে তরল ইথেন বাব্যহৃত হয়।
(৫) https://www.youtube.com/watch?v=026rzTXb1zw
(৬) J. Chem. Educ. 2014, 91, 2009−2012
(৭) Science News 2017, 192, 6.
(8) Nature, 2015, 525, 172–174.
(৯) BBA – General Subjects 2018, 1862, 324–334
(১০)https://www.chemistryworld.com/news/explainer-what-is-cryo-electron-microscopy/3008091.article
(১১)https://phys.org/news/2017-10-nobel-winning-technique-google-earth-molecules.html(১২) Mol. Cancer Ther. 2009, 8, 626.