এই বছর চিকিৎসা বিজ্ঞানে নোবেল পুরস্কার দিয়ে যাদের সম্মানিত করা হল, তারা সকলেই পরজীবী বা প্যারাসাইট (parasite) জনিত রোগের মোকাবিলায় নজির স্থাপন করেছেন। এদের দ্বারা প্রবর্তিত চিকিৎসা পদ্ধতি যে কত মানুষের প্রাণ বাঁচিয়েছে, তার হিসেব মেলা ভার! আজকের লেখার বিষয় তাদেরই একজনকে নিয়ে: চীনের মহিলা বিজ্ঞানী, ইয়উয়উ টু। চীনের প্রাচীন চিকিৎসা পদ্ধতির ব্যবহারিক জ্ঞান কাজে লাগিয়ে, ষাট-সত্তরের দশকে, ম্যালেরিয়া রোগের চিকিৎসায় তিনি এক বিপ্লব ঘটিয়েছিলেন।

প্রথমেই প্রশ্ন আসে: ম্যালেরিয়ার চিকিৎসা তো সাড়ে তিনশো বছর ধরে চলে আসছে, প্রোফেসর টু নতুন কি করলেন? এমন তো নয় যে ষাট-সত্তরের দশকের আগে ম্যালেরিয়া হওয়া মানেই নির্ঘাত মৃত্যু ছিল! সেই গল্প জানতে হলে, আগে ম্যালেরিয়া রোগ আর তা নিরাময়ের জন্যে ব্যবহৃত নানা রকমের ওষুধের জৈবরাসায়নিক ক্রিয়া পদ্ধতির কথা জানা দরকার।
ম্যালেরিয়ার আদি শত্রু: কুইনিন
কিছু বিশেষ মশার কামড়ে য়ে ম্যালেরিয়া হয়, তা আমরা সকলেই জানি। রোগের উপসর্গ সর্বাঙ্গে কাঁপুনি দিয়ে জ্বর, আর অনেক ক্ষেত্রেই পরিনতি মারাত্মক! বহুকাল আগে থেকেই পেরু এবং বলিভিয়ার মত দেশে, কাঁপুনি দিয়ে জ্বর এলেই সিনকোনা গাছের ছালের রস খাইয়ে মানুষের প্রাণ বাঁচানো হত। লক্ষণীয় বিষয়, ঠিক একই সময়ে চীনদেশেও সেই জ্বরের চিকিৎসা করা হত সুইট ওয়ার্মউড গাছের পাতার রস দিয়ে।
১৮২০ সালে ফরাসি বিজ্ঞানীরা দেখান যে সিনকোনা গাছের ছালে কুইনিন নামে একটা পদার্থ ম্যালেরিয়া রোগ সারায়।

গাছের নির্যাস খাইয়ে চিকিৎসা করা গেলেও সেই গাছ পৃথিবীর সব দেশে পাওয়া যেত না। গাছের ছালের আমদানি করেও চাহিদা মেটানো সহজ ছিল না। ১৮২০ সালে ফরাসি বিজ্ঞানীরা বের করেন যে সিনকোনা গাছের ছালের রসে কুইনিন নামে একটা জৈবরাসায়নিক পদার্থ আছে। গাছের ছালের মধ্যে থাকা এই কুইনিনই আসলে ম্যালেরিয়া রোগ সারায়। এই তথ্যটা জানার পরেই কুইনিনের মত রাসায়নিক পদার্থ বানানো শুরু হয়ে গেল বিভিন্ন গবেষণাগারে। তার ফলে আবিষ্কার হল অনেকগুলো ওষুধ, যাদের মধ্যে সব থেকে বেশি সাফল্য পেল ক্লোরোকুইন। ১৯৩৪ সালে ক্লোরোকুইনের আবিষ্কারের পর থেকে সমস্ত দেশে এর ব্যাপক ব্যবহার শুরু হল।
কিন্তু, ১৯৫০ সালের পর থেকেই দেখা গেল যে এই ওষুধ বেশ কিছু ক্ষেত্রে কাজ করছে না। কারণ: অতিরিক্ত মাত্রায় ক্লোরোকুইনের ব্যবহার। দুই-তিন দশকের মধ্যেই, পৃথিবীর সমস্ত ম্যালেরিয়া-প্রবণ দেশে দেখা গেল ক্লোরোকুইন তার কার্যক্ষমতা হারিয়েছে। ফলে ম্যালেরিয়া-জনিত রোগে মৃত্যুর হার বেড়ে গেল দুই-তিন গুণ।
ম্যালেরিয়া সারাতে যুদ্ধকালীন তৎপরতা
এরই মাঝে ১৯৫৫ সালে শুরু হয়ে গেল ভিয়েতনাম যুদ্ধ। উত্তর ভিয়েতনাম লড়ছিল দক্ষিণ ভিয়েতনাম এবং আমেরিকার বিরুদ্ধে। মানুষের পরিকল্পিত যুদ্ধের মাঝে, সামরিক বাহিনীর মধ্যে ভীষণ আতঙ্ক হয়ে দাড়ালো ম্যালেরিয়া। দরকার হয়ে পড়ল দ্রুত রোগ নিরাময়ের। নিরূপায় উত্তর ভিয়েতনামের দিকে সাহায্যের হাত বাড়িয়ে দিল চীন। ২৩ মে, ১৯৬৩ সালে চীন শুরু করলো এক গোপন প্রকল্প – “প্রজেক্ট ৫২৩”।
সেই “প্রজেক্ট ৫২৩”-তেই যোগ দেন ইয়উয়উ টু এবং আরও অনেক বিজ্ঞানী। ১৯৭০ সালে সুইট ওয়ার্মউড গাছড়ার নির্যাসে পাওয়া গেল আরটেমিসিনিন (Artemisinin) নামের একটি পদার্থ। চীনা ভাষায় এর নাম চিংহাউসু (qinghaosu)। আরটেমিসিনিন ম্যালেরিয়ার বিরুদ্ধে কাজ করতে সক্ষম। কিন্তু পদার্থটা ব্যবাহারযোগ্য অবস্থায় এই গাছড়া থেকে উদ্ধার করাটা মোটেই সহজ কাজ ছিল না।
সমস্যা ছিল তখনকার প্রচলিত রাসায়নিক নিষ্কাশন পদ্ধতি। যে তাপমাত্রায় রাসায়নিক পৃথকীকরণ করা হচ্ছিল, সেই তাপমাত্রায় আরটেমিসিনিনের কার্যক্ষমতা যাচ্ছিল অনেক কমে। ইয়উয়উ টু এবং তাঁর সহকর্মীরা জয়লাভ করলেন সেখানেই। তাঁরা এক নতুন পদ্ধতির উদ্ভাবন করলেন, যার দ্বারা রাসায়নিক ভাবে আরটেমিসিনিনের নানান সক্রিয় যৌগ নিষ্কাশন করা সম্ভব হলো1।
ব্যবহার করো কিন্তু সামলে
নব্বইয়ের দশকের প্রথম দিকে, ক্লোরোকুইন কাজ না করলে প্রয়োগ করা হত আরটেমিসিনিন যৌগগুলোর একটা পাঁচ-মেশালী বা আরটেমিসিনিন বেসড কম্বিনেশন থেরাপি (ACT)। ACT-র মধ্যে থাকতো:
(১) যে কোনও একটা আরটেমিসিনিনের যৌগ, এবং
(২) অন্য কোনও ক্লাসের অ্যান্টি-ম্যালেরিয়াল ওষুধ যেমন লুমেফ্যানট্রিন, মেফ্লোকুইন, অ্যামোডায়াকুইন, ইত্যাদি।
ACT-এর মধ্যে আরটেমিসিনিন যৌগের কাজ হচ্ছে প্রথম তিন দিনের মধ্যেই রক্তের মধ্যে থাকা বেশীর ভাগ পরজীবীর সংখ্যা কমানো। অপর ওষুধটি বাকি বেঁচে থাকা পরজীবীদের মেরে ফেলে।
এই থেরাপির সুবিধে এটাই যে এতে আরটেমিসিনিন যৌগ প্রয়োগের মাত্রাটা কম রাখা সম্ভব। চিকিৎসা পদ্ধতিতে এর বেশ একটা লাভজনক দিকও রয়েছে। ওষুধের পার্শ্ব পতিক্রিয়া তো কম থাকেই। তাছাড়া আরটেমিসিনিন কম পরিমাণে ব্যবহার করলে তার কার্যক্ষমতা অনেক বেশি দিন থাকে। কারণ আর কিছুই না, আরটেমিসিনিন-প্রতিরোধী পরজীবীদের ছড়াতে অনেক বেশি সময় লাগে। অন্তত এমনটাই বিজ্ঞানীদের অনুমান।
সুইট ওয়ার্মউড গাছড়ার নির্যাসে ইয়উয়উ টু এবং তাঁর সহকর্মীরা পেলেন ‘আরটেমিসিনিন’, যা ক্লোরোকুইন প্রতিরোধী ম্যালেরিয়ার বিরুদ্ধে কাজ করতে সক্ষম।
বর্তমানে ৭৯টি দেশে ACT-কে প্রথম সারির চিকিৎসাপদ্ধতি হিসেবে ব্যাবহার করা হয়। ওয়ার্ল্ড হেলথ অর্গ্যানাইজেশন (WHO)-এর রিপোর্ট 2 অনুযায়ী ACT-র ব্যবহারের ফলে ম্যালেরিয়ায় মৃত্যুর হার তিরিশ শতাংশ কমেছে। তাহলে বুঝতেই পারছ যে ম্যালেরিয়ার চিকিৎসায় আরটেমিসিনিন অত্যন্ত গুরুত্বপূর্ণ আবিষ্কার।
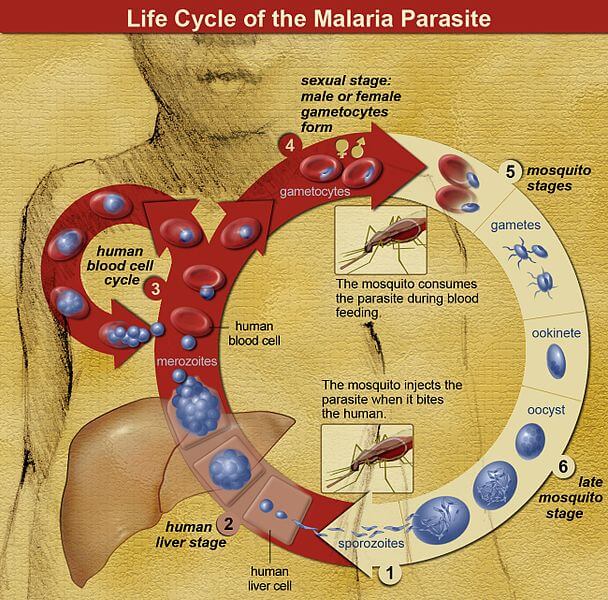
ম্যালেরিয়া জীবাণুর জীবনচক্র
কুইনিন কোথায় ব্যর্থ হলো আর আরটেমিসিনিন কেন সফল, সেটা বুঝতে হলে ম্যালেরিয়ার সংক্রমণ পদ্ধতি সম্বন্ধে একটু গভীরে ঢুকতে হবে।
মানুষের মধ্যে ম্যালেরিয়ার জন্য দায়ী প্লাসমোডিয়া গোত্র বা ‘জেনাস’-এর পরজীবী। প্লাসমোডিয়াম ফ্যালসিপেরাম আর প্লাসমোডিয়াম ভাইভ্যাক্স – এই দুটো পরজীবী ম্যালেরিয়া-জনিত মৃত্যুর প্রধান কারণ। পরজীবীর প্রবেশ থেকে শুরু করে তার প্রজনন, পুরো চক্রটা খানিকটা এইরকম হয়।
১। লিভার দশা (liver stage): স্ত্রী অ্যানোফিলিস মশা পরজীবীকে শরীরের মধ্যে প্রবেশ করিয়ে দেয়। মুহূর্তের মধ্যেই সে যকৃত বা লিভার-এর কোষের ভিতরে গা ঢাকা দেয়। এই দশায় থাকাকালীন পরজীবীরা আমাদের কোনও জানান দেয় না।
২। রক্ত দশা (blood stage): এরপর পাঁচ-ছ’দিনের মধ্যেই পরজীবীরা যকৃত থেকে লোহিত রক্ত কণিকায় নিজেদের জায়গা বানিয়ে ফেলে। এই দশাতেই শারীরিক জটিলতা শুরু হয়। কাঁপুনি দিয়ে জ্বর আসাটা এই সময়েই হয়ে থাকে। পরজীবীরা রক্ত কণিকার ভিতরে থাকা হিমোগ্লোবিন ভেঙে গ্লোবিন প্রোটিনকে নিজেদের বিপাকীয় প্রক্রিয়ায় ব্যবহার করতে শুরু করে। এইভাবে তাদের জীবনচক্র এগোতে থাকে। আর এই কারণেই এরা পরজীবী: শত হলেও, মানব দেহে হিমোগ্লোবিন তো আর এদের পুষ্টির জন্য তৈরী হয়নি!
হিমোগ্লোবিন ভাঙার এই ঘটনা ঘটে পরজীবীর ভিতরে থাকা খাদ্য থলির মধ্যে। হিমোগ্লোবিন ভাঙার পরে গ্লোবিন ব্যবহার হলেও, খাদ্য থলির ভিতরে অবশিষ্ট থাকে হিম (Heme)। এই হিম অণু পরজীবীদের কাছে খুব ক্ষতিকারক (নিচে, টীকা ১ দেখো)। পরজীবীরা তাই চটপট এই হিমকে হিমোজইন নামক পদার্থে পরিবর্তন করে ক্ষতিকারক হিমের হাত থেকে রক্ষা পায়।
৩। গ্যামেটোসাইট দশা (gametocyte stage): শুধু খেয়েদেয়েই শান্তি নেই, এবার ম্যালেরিয়ার পরজীবীরা বংশবিস্তার করতে শুরু করে। গ্যামেটোসাইট মানে হল জননকোষ। পুরুষ এবং স্ত্রী গ্যামেটোসাইট, উভয়েই ম্যালেরিয়া রোগীর রক্তে তৈরি হয়। ম্যালেরিয়া রোগী নতুন করে মশার কামড় খেলে রক্তে থাকা এই গ্যামেটোসাইট আবার মশার মধ্যে প্রবেশ করে। মশার দেহের মধ্যে পরজীবীর যৌন জনন (sexual stage) শেষ হলে উৎপন্ন হয় নবজাতক, যা আবার সেই মশার কামড়ে অন্য মানুষের শরীরে প্রবেশ করে।
কুইনিন যৌগ কোথায় বাধ সাধে
তাহলে দাড়ালো এই যে, ম্যালারিয়ার পরজীবীকে আটকাতে হলে এই দশাগুলির কোনো একটাকে সফল হওয়া থেকে আটকাতে হবে। এখনও পর্যন্ত সব থেকে সফল অ্যান্টি-ম্যালেরিয়াল ওষুধগুলি, যেমন ক্লোরোকুইন, মেফ্লোকুইন, ইত্যাদি পরজীবীদের রক্ত দশাকেই আক্রমণ করেছে। ক্লোরোকুইন পরজীবীর খাদ্য থলিতে প্রবেশ করে হিম থেকে হিমোজোইন তৈরীর রাসায়নিক প্রক্রিয়াকে বাধা দেয়। পরজীবীদের ভিতরে হিম-এর পরিমাণ বৃদ্ধি পায়, আর এই হিম-এর বিষক্রিয়ায় তাদের মরতে হয়।
আর এইখানেই যত বিপত্তি। কিছু পরজীবীর এমন পরিবর্তন ঘটেছে যে তারা ক্লোরোকুইনকে নিজেদের খাদ্যথলির ভিতর জমতেই দেয় না। ফলে তারা দিব্বি বেঁচে-বর্তে থাকে (নিচে, টীকা ২ দেখো)। শুধু ক্লোরোকুইন নয়, আরও কিছু অ্যান্টিম্যালেরিয়াল ওষুধকেও একই সাথে প্রতিরোধ করতে পারছে ওই সব মাল্টিড্রাগ রেসিস্ট্যান্ট (MDR) পরজীবী।
আর এখানেই আরটেমিসিনিনের এর গুরুত্ব, কারণ আরটেমিসিনিন এইসব প্রতিরোধী পরজীবীদের অনায়াসেই মারতে পারে। ঠিক কিভাবে আরটেমিসিনিন কাজ করে?
মুশকিল আসানকারী আরটেমিসিনিন
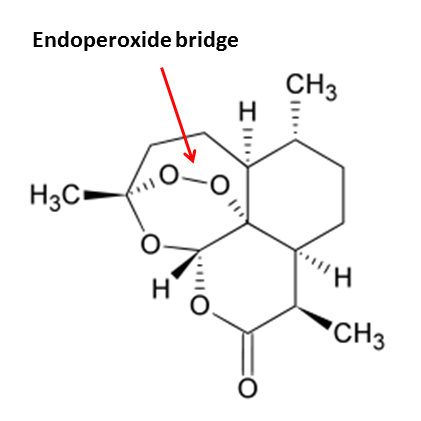
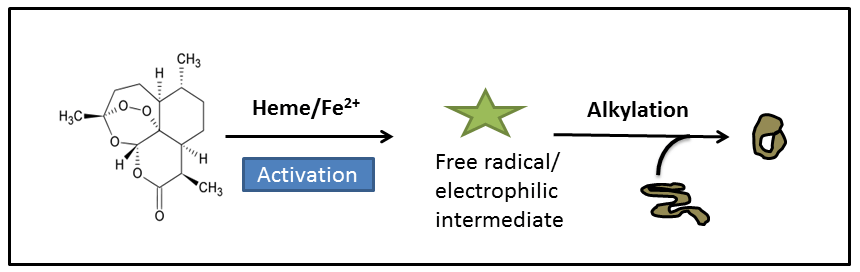
রাসায়নিকভাবে আরটেমিসিনিন হল সেসকিটার্পিন ল্যাকটোন (sesquiterpene lactone) নামের একটি যৌগ। কেমিকাল ফর্মুলা C15H22O5। এর কাঠামো লক্ষ্য করলে দেখবে, ভিতরে থাকে যাকে বলে একটা এন্ডোপারক্সাইড ব্রিজ (endoperoxide bridge)। বিজ্ঞানীরা প্রমাণ করেছেন আরটেমিসিনিন এর ম্যালেরিয়া-বিনাশক ক্ষমতার জন্যে আসলে এই এন্ডোপেরক্সাইড ব্রিজ-ই দায়ী।
বিজ্ঞানীরা মনে করেন যে আরটেমিসিনিন একটা প্রোড্রাগ (prodrug) যা একবার রক্ত কণিকায় থাকা পরজীবীর ভিতরে প্রবেশ করলে, তবেই সে একটা সক্রিয় পদার্থে পরিবর্তিত হয় এবং সেইটিই আসলে পরজীবী মারার কাজ করে।
অর্থাৎ, আরটেমিসিনিন দুটো ধাপে কাজ করে। প্রথম ধাপ হলো সক্রিয়করণ বা এক্টিভেশন (activation)। সাধারনভাবে মনে করা হয় যে, পরজীবীর ভিতর প্রবেশ করার পরে আরটেমিসিনিন আয়রন (Fe2+) অথবা ফেরাস হিম-এর সাথে বিক্রিয়া করে। তৈরী হয় একটা মাঝামাঝি সক্রিয় অবস্থা। দ্বিতীয় ধাপে, এই মাঝামাঝি অবস্থার পদার্থটি পরজীবীর কিছু প্রোটিনের অ্যালকাইলেশন (alkylation) করে প্রোটিনগুলোকে নিষ্ক্রিয় করে দেয়।
পরজীবীর শরীরে নানান রাসায়নিক প্রক্রিয়া সুসম্পন্ন করার জন্য এইসব প্রোটিনের খুবই প্রয়োজন। এদের নিষ্ক্রিয় হয়ে যাওয়ার ফলেই পরজীবীর মৃত্যু হয়। তবে আরটেমিসিনিন কিভাবে কাজ করে, সেই নিয়ে বিজ্ঞানী মহলে এখনও নানা রকম তত্ত্ব উঠে আসছে। কোনটা কতটা ঠিক, তা এখনই জোর দিয়ে বলা মুশকিল।
আরটেমিসিনিন-এর দিন কি ফুরিয়ে এলো ?
আরটেমিসিনিন কতদিন সফল থাকবে বলে তোমাদের ধারণা ? আরও দশ-কুড়ি বছর? আমাদের জানা নেই। তবে তোমরা শুনলে চমকে উঠবে, বর্তমানে পাঁচটি দেশে (কাম্বোডিয়া, লাওস, মায়ানমার, থাইল্যান্ড ও ভিয়েতনাম) আরটেমিসিনিন প্রতিরোধে সক্ষম পরজীবীর খোঁজ পাওয়া গেছে। দুঃখের কথা, আমাদের হাতে মজুদ থাকা অস্ত্র দিয়ে এদের মারা যাচ্ছে না 3।
ঠিক এই কারণেই আরটেমিসিনিন বেসড কম্বিনেশন থেরাপির ব্যাবহার করা হচ্ছে। আরটেমিসিনিন কম পরিমাণে ব্যবহার করলে তার কার্যক্ষমতা অনেক বেশি দিন বজায় থাকবে। আর ওই আরটেমিসিনিন প্রতিরোধে সক্ষম পরজীবীদের ছড়াতে অনেক সময় লাগবে। এমনটাই বিজ্ঞানীদের অনুমান 4। (নিচে, টীকা ৩ দেখো)
ভবিষ্যতে কোন ওষুধ ম্যালেরিয়া থেকে আমাদের বাঁচাতে পারবে, তা এখনই বলা সম্ভব নয়। বিজ্ঞানীদের তৎপরতায় কিছু নতুন অণুর খোঁজ পাওয়া গেছে, যা ভবিষ্যতে সফল ম্যালেরিয়ার ওষুধের জায়গা নিতেই পারে। কিন্তু এই ওষুধগুলোকে অনেক বছর কার্যকর রাখাটাই বিজ্ঞানীদের কাছে অনেক বেশী চ্যালেঞ্জিং। ম্যালেরিয়ার টীকা আবিষ্কার হওয়াটা খুবই প্রয়োজন। আর যতদিন তা না হচ্ছে, ম্যালেরিয়া-বিনাশকারী ওষুধই আমাদের ভরসা।
টীকা :
১) কেন রক্তের হিমোগ্লোবিন ভেঙ্গে অবশিষ্ট হিম পরজীবীদের কাছে ক্ষতিকারক:
হিমোগ্লোবিন থেকে বেরিয়ে আসা ফ্রি হিম লিপোফিলিক (Lipophilic)। তাই খুব সহজেই খাদ্যথলি থেকে বেরিয়ে এসে কোষ পর্দায় ছিদ্র করে কোষ পর্দাকে ভেঙে দিতে পারে। এছারা ফ্রি হিম হাইড্রোজেন পারক্সাইডের(H2O2) সাথে বিক্রিয়া করে হাইড্রক্সিল মূলক (OH–)-এর মত সক্রিয় জারক তৈরি করতে পারে। এই সক্রিয় জারক পরজীবীদের DNA-র ক্ষতি করতে পারে এবং নানা রকম প্রয়োজনীয় লিপিড ও প্রোটিনকে জারিত (oxidize) করে তাদের মেরে ফেলতে পারে। প্রচুর জারণক্ষম রাসায়নিক (free oxidants) তৈরি হয়ে কোষের মধ্যে যে ক্ষতিকারক পরিস্হিতির সৃষ্টি হয় তাকে অক্সিডেটিভ স্ট্রেস (oxidative stress) বলা হয়। তাই হিম-এর থেকে নিজেকে রক্ষা করতে পরজীবী হিম অণুগুলোকে জোড়া লাগিয়ে বা পলিমারাইজ (polymerize) করে হিমোজোইন (Hemozoin) এ পরিনত করে, যে হিমোজোইন (Hemozoin) তাদের আর কোনও ক্ষতি করতে পারে না।
২) কেন কিছু পরজীবী ক্লোরোকুইনকে পাত্তা দেয় না:
ক্লোরোকুইন একটি দুর্বল ক্ষার যা খাদ্য থলির ভিতরে সহজেই প্রবেশ করতে পারে। এই ক্লোরোকুইন একবার অ্যাসিডিক খাদ্যথলিতে প্রবেশ করলে তার প্রোটনেশন (protonation) হয়। এর ফলে ক্লোরোকুইন খাদ্য থলিতে আটকা পরে। কিন্তু ক্লোরোকুইন প্রতিরোধে সক্ষম পরজীবীদের মধ্যে এমনই পরিবর্তন ঘটেছে যে খাদ্য থলির ভিতর ক্লোরোকুইন সঠিক পরিমাণে জমতে পারে না। এই পরিবর্তনের কারণ PfCRT (প্লাসমোডিয়াম ফ্যালসিপ্যারাম ক্লোরোকুইন রেসিস্ট্যান্ট ট্রান্সপোর্টার) জিন-এ মিউটেশন। কিন্তু ঠিক কিভাবে এই মিউটেশন পরজীবীদের ক্লোরোকুইন প্রতিরোধ সক্ষম করে তুলছে, তা এখনও স্পষ্ট নয়। PfCRT প্রোটিনটি খাদ্য থলির পর্দার ওপরে থাকে আর কোনও এক অজ্ঞাত পদ্ধতিতে ক্লোরোকুইনকে খাদ্য থলির বাইরে বার করে দেয়।
৩) কেন আরটেমিসিনিন অল্পমাত্রায় ব্যবহার করলে অনেকদিন চলার সম্ভাবনা আছে:
সাধারণভাবে পরজীবীদের জিনে পরিবর্তন হওয়ার প্রবণতা বেশ কম। একটা পরিক্ষায় দেখা গেছে যে DHFR নামক জিনে পরিবর্তনের হার হল 10-9 mutations/DHFR gene/replication। পরিবর্তনের হার বেশি হলে যেমন প্রতিরোধী হওয়ার সম্ভবনাও বারে, আবার খারাপ পরিবর্তনের ফলে পরজীবীদের ক্ষতি হওয়ার এবং মারা যাওয়ার সম্ভবনাও আরও বেশি হয়। তাই খুব বেশি পরিবর্তনের হার কখনই কাম্য নয়। পরিবর্তনের হার কম হওয়া সত্ত্বেও সিলেকশন প্রেসারের ফলে পরিবর্তিত পরজীবী তৈরি হয়। ইনফেকশন-এর পর চিকিৎসার সময় যে পরিমাণ ওষুধের প্রয়োজন হয়, রক্তে থাকা সমস্ত পরজীবীদের মারতে সেই পরিমাণ ওষুধে এই পরিবর্তিত পরজীবীরা বেঁচে যায়। এই পরজীবীগুলির গ্যামেটোসাইট দশায় রুপান্তরিত হলেই আবার মশার মধ্যে প্রবেশ করে এবং এইভাবে পরিবর্তিত প্রতিরোধী পরজীবীরা ছড়িয়ে পরে। নির্বিচারে ওষুধের ব্যবহার, ওষুধের ভুল পরিমাণ বা ডোস, নকল ওষুধের ব্যবহার, ইত্যাদি নানা রকম কারণে এই সিলেকশন প্রেসারের পরিবর্তন হচ্ছে। এর ফলে পরজীবীদের প্রতিরোধী হওয়ার প্রবণতা বেড়ে যাচ্ছে। তাই যথেচ্ছভাবে ওষুধের ব্যবহার না করা এবং ডোস-এর পরিবর্তন না করাই বাঞ্ছনীয় 5।
লেখার উৎস:
- The discovery of artemisinin (qinghaosu) and gifts from Chinese medicine. Nature Medicine 17, 1217–1220 (2011)
- WHO Malaria Report 2014
- WHO Malaria Report (updated February 2015): https://who.int/malaria/media/artemisinin_resistance_qa/en/
- Artemisinin-based combination therapies: a vital tool in efforts to eliminate malaria. Nature Reviews Microbiology 7, 864-874 (December 2009)
- Drug-resistant malaria: molecular mechanisms and implications for public health. FEBS Lett. 2011 Jun 6;585(11):1551-62.